دو عامل مهم موثر در آنتروپی عبارتند از :
۱- دما : هر چه دما افزایش یابد ، جنبش ذرات ماده بیشتر شده و آنتروپی افزایش می یابد . (دما با آنتروپی رابطه مستقیم دارد )
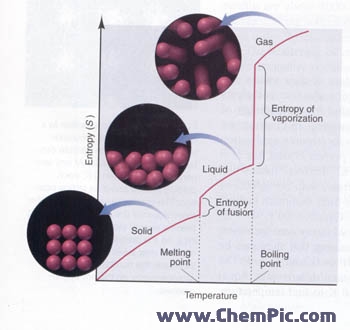
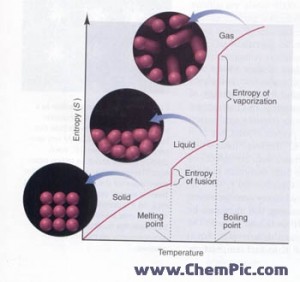
۲- تغییر حالت : با تغییر حالت از جامد به مایع ( ذوب ) و از مایع به گاز ( تبخیر )، آزادی حرکت ذرات ماده بیشتر شده و آنتروپی افزایش می یابد . میزان تغییر آنتروپی هنگام تبخیر بیشتر تغییر آنتروپی هنگام ذوب شدن است.
تصویر نمودار تغییرات آنتروپی نسبت به دما را از صفر درجه کلوین تا بالاتر از نقطه جوش نشان می دهد . در صفر کلوین آنتروپی صفر است و با افزایش دما آنتروپی افزایش می یابد. در نقطه ذوب و جوش ، نمودار بصورت عمودی افزایش می یابد زیرا در نقطه ذوب و جوش دما ثابت است ولی انتروپی به علت تغییر حالت افزایش می یابد و تغییر آنتروپی هنگام جوش بیشتر از تغییر آنتروپی هنگام ذوب است .
 شیمی دبیرستان و کنکور :: Chem-Pic :: آموزش شیمی
شیمی دبیرستان و کنکور :: Chem-Pic :: آموزش شیمی